Tout vaccin repose sur le même mensonge fondamental : il convainc votre système immunitaire qu’un agent pathogène dangereux est arrivé, sans le danger réel. Ce qui se produit ensuite est l’un des processus biologiques les plus sophistiqués du corps humain, un exercice d’entraînement en plusieurs étapes qui laisse vos défenses durablement renforcées contre une menace qu’elles n’ont peut-être jamais vraiment rencontrée.
Comprendre ce mécanisme dépasse la simple curiosité académique. À l’heure des vaccins à ARNm, des débats sur la préparation aux pandémies et des questions croissantes sur les calendriers de rappel, la machinerie moléculaire derrière l’immunité acquise n’est plus du seul ressort de l’immunologie. C’est une infrastructure publique.
La première alarme : comment votre organisme détecte un vaccin
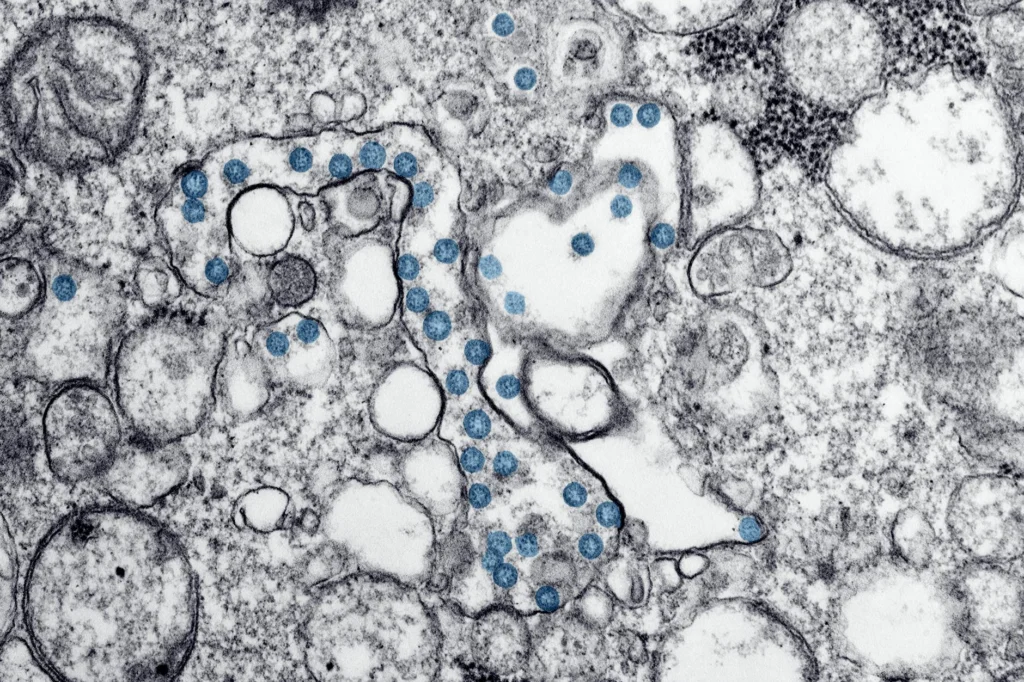
En quelques minutes après l’injection, votre système immunitaire inné, la branche plus ancienne et moins spécifique de l’immunité, détecte le vaccin grâce aux récepteurs de reconnaissance de motifs (PRR). Ces récepteurs, notamment la famille des récepteurs de type Toll (TLR), recherchent les signatures moléculaires associées aux agents pathogènes : protéines étrangères, lipides ou acides nucléiques qui n’ont pas leur place dans les tissus sains.
Il ne s’agit pas d’une réponse ciblée. Le système immunitaire inné ne sait pas quel agent pathogène spécifique est arrivé. Il reconnaît simplement la présence d’un élément étranger et déclenche l’alarme. Les cellules immunitaires au site d’injection, notamment les cellules dendritiques et les macrophages, commencent à engloutir les composants du vaccin. Elles découpent les protéines en petits fragments appelés peptides et les exposent à leur surface grâce à des molécules appelées CMH (complexe majeur d’histocompatibilité).
On peut imaginer un système d’« avis de recherche ». Les cellules dendritiques transportent ces avis moléculaires du site d’injection vers le ganglion lymphatique le plus proche, où le véritable entraînement commence.
Le passage de relais : de l’immunité innée à l’immunité adaptative
Le ganglion lymphatique est le lieu où les immunités innée et adaptative se rencontrent. Les cellules dendritiques présentent leurs fragments peptidiques liés au CMH aux lymphocytes T, des globules blancs spécialisés capables de reconnaître des formes moléculaires d’une précision remarquable. Chaque lymphocyte T porte un récepteur unique à sa surface, et parmi les milliards de lymphocytes T dans votre organisme, seule une poignée correspond au peptide présenté.
Lorsqu’une correspondance se produit, ce lymphocyte T s’active. Il commence à se diviser rapidement, produisant une armée de cellules identiques. Certains deviennent des lymphocytes T « auxiliaires » (CD4+), qui coordonnent la réponse immunitaire globale. D’autres deviennent des lymphocytes T « tueurs » (CD8+), capables de détruire directement les cellules affichant la protéine étrangère.
Les lymphocytes T auxiliaires sont particulièrement cruciaux car ils activent les lymphocytes B, un autre type de cellule immunitaire qui produit des anticorps. Sans les signaux des lymphocytes T auxiliaires, la plupart des lymphocytes B ne peuvent pas monter une réponse anticorps robuste. Cette coopération entre types cellulaires explique pourquoi les adjuvants dans les vaccins agissent en renforçant à la fois la présentation des antigènes et les signaux co-stimulateurs qui consolident ces échanges intercellulaires.
L’usine à anticorps : les lymphocytes B et les centres germinatifs
Une fois activés par les lymphocytes T auxiliaires, les lymphocytes B traversent l’un des processus les plus remarquables de la biologie. Ils migrent vers des structures spécialisées du ganglion lymphatique appelées centres germinatifs, où ils entrent dans un cycle de mutations rapides et de sélection qui reproduit l’évolution en accéléré.
Dans le centre germinatif, les lymphocytes B se divisent rapidement tout en introduisant des mutations aléatoires dans les gènes codant leurs récepteurs d’anticorps. Ce processus, appelé hypermutation somatiqueProcessus par lequel les lymphocytes B mutent rapidement leurs gènes d'anticorps pour affiner leur précision et leur affinité., est un chaos contrôlé. La plupart des mutations sont inutiles ou même nuisibles. Mais certaines produisent des anticorps qui se lient à leur cible plus étroitement qu’auparavant.
Les lymphocytes B portant des anticorps améliorés reçoivent des signaux de survie des lymphocytes T auxiliaires. Ceux dotés d’anticorps plus faibles n’en reçoivent pas et meurent. Au fil des jours et des semaines, ce processus de sélection darwinienne produit des anticorps de qualité croissante. C’est pourquoi les anticorps produits par votre organisme après un rappel sont généralement plus efficaces que ceux de la première dose : ils ont été affinés à travers de multiples cycles de mutations et de sélection.
La mémoire : le véritable objectif
Le produit ultime de la vaccination n’est pas la réponse immunitaire initiale. C’est la mémoire. Après l’élimination des composants du vaccin et la dissipation de la réponse aiguë, deux populations de cellules à longue durée de vie subsistent.
Les lymphocytes B mémoire sont des sentinelles qui peuvent persister des années, voire des décennies. S’ils rencontrent à nouveau le même agent pathogène, ils se différencient rapidement en cellules productrices d’anticorps, générant une réponse plus rapide et plus forte qu’au premier contact. Alors qu’une réponse immunitaire primaire prend environ deux semaines pour produire des anticorps détectables, une réponse mémorielle les génère en seulement deux à quatre jours.
Les lymphocytes T mémoire fonctionnent de manière similaire. Après l’activation initiale, le nombre de lymphocytes T spécifiques à l’agent pathogène chute fortement mais se stabilise à un niveau 100 à 1 000 fois supérieur à celui d’avant la vaccination, persistant tout au long de la vie. Ces cellules ne sont pas seulement plus nombreuses. Elles sont pré-armées, nécessitent moins de stimulation pour se réactiver et sont capables de monter une réponse avant que l’agent pathogène ne s’établisse.
Les plasmocytes à longue durée de vie ajoutent un troisième niveau de protection. Ces cellules, qui résident principalement dans la moelle osseuse, sécrètent en continu de faibles niveaux d’anticorps pendant des décennies, même sans nouvelle exposition à l’antigène. C’est pourquoi une seule vaccination contre la rougeole dans l’enfance peut assurer une protection à vie.
Pourquoi les rappels sont efficaces
Une dose de rappel réactive les cellules mémoire générées par les vaccinations précédentes. Les lymphocytes B mémoire retournent dans les centres germinatifs et subissent des cycles supplémentaires de mutations et de sélection, augmentant encore l’affinité des anticorps à chaque immunisation successive. Le résultat est des anticorps non seulement plus abondants, mais aussi plus efficaces pour neutraliser l’agent pathogène.
Les rappels élargissent également la population de lymphocytes T mémoire. Des recherches sur les vaccins à ARNm contre la COVID-19 ont montré que l’immunisation secondaire produisait une augmentation frappante des lymphocytes T CD8+ spécifiques à l’antigène, notamment dans les poumons, l’un des principaux sites d’infection respiratoire.
La révolution ARNm
Les vaccins traditionnels utilisent des agents pathogènes atténués ou inactivés, ou des protéines purifiées, pour déclencher une réponse immunitaire. Les vaccins à ARNm adoptent une approche fondamentalement différente. Au lieu de livrer un antigène prêt à l’emploi, ils livrent des instructions génétiques, enveloppées dans des nanoparticules lipidiquesMinuscules particules graisseuses utilisées pour encapsuler et délivrer du matériel génétique dans les cellules, notamment vers le foie. composées de quatre types de lipides : lipides ionisables, lipides auxiliaires, cholestérol et lipides conjugués au PEG.
Une fois à l’intérieur d’une cellule, l’ARNm est traduit par la machinerie de synthèse protéique propre à la cellule en l’antigène cible (pour les vaccins contre la COVID-19, la protéine spike). Parce que la protéine est produite à l’intérieur de la cellule plutôt que livrée de l’extérieur, elle est traitée par la même voie que l’organisme utilise pour les cellules infectées par un virus. Cela signifie qu’elle est présentée sur les molécules CMH de classe I, activant fortement les lymphocytes T tueurs en plus de la réponse anticorps.
C’est un avantage clé. Les vaccins à ARNm induisent efficacement à la fois les lymphocytes T cytotoxiques et les lymphocytes T mémoire résidents dans les tissus grâce à la présentation endogène de l’antigène, ce qui est plus difficile à obtenir avec les vaccins inactivés traditionnels.
Au-delà de la protection individuelle : l’immunité entraînéeCapacité des cellules immunitaires innées à répondre plus efficacement à de futures infections après une exposition antérieure, sans mémoire classique par anticorps.
L’une des découvertes les plus surprenantes de l’immunologie récente est que certains vaccins semblent également entraîner le système immunitaire inné, et pas seulement le bras adaptatif. Ce phénomène, appelé immunité entraînée, implique des modifications durables des cellules immunitaires innées par reprogrammation épigénétique et métabolique.
Le vaccin BCG (contre la tuberculose) est l’exemple le plus étudié. Les personnes vaccinées avec le BCG montrent une résistance renforcée non seulement à la tuberculose, mais aussi à des infections sans rapport, suggérant que le vaccin induit un système immunitaire inné plus largement vigilant. Il ne s’agit pas de la mémoire immunologique classique. Elle fonctionne par des mécanismes entièrement différents, modifiant la façon dont les gènes dans les cellules immunitaires innées sont lus sans changer la séquence ADN elle-même.
Ce qui peut dysfonctionner
Aucun système aussi complexe ne fonctionne parfaitement à chaque fois. Certaines personnes génèrent des réponses immunitaires plus faibles en raison de l’âge, d’une immunosuppression ou d’une variation génétique. Les personnes âgées, en particulier, ont tendance à produire moins de réactions dans les centres germinatifs et des anticorps de moindre qualité, ce qui explique pourquoi les formulations vaccinales pour les adultes plus âgés incluent souvent des adjuvants plus puissants.
Les agents pathogènes peuvent également évoluer pour échapper à la mémoire immunitaire. La grippe mute ses protéines de surface si rapidement que les anticorps de l’année précédente peuvent ne pas reconnaître la souche de cette année. Les variants du SRAS-CoV-2 portant des mutations dans la protéine spike peuvent partiellement échapper aux anticorps générés contre les souches antérieures. Cependant, les lymphocytes T ciblant les régions virales conservées maintiennent leur reconnaissance à travers les variants, ce qui explique pourquoi les personnes vaccinées sont encore largement protégées contre les maladies graves même quand l’efficacité des anticorps diminue.
C’est un point crucial souvent perdu dans le débat public : les anticorps ne sont pas la seule mesure de la protection vaccinale. L’immunité lymphocytaire T fournit une deuxième ligne de défense durable que les agents pathogènes ont plus de mal à contourner.
Cet article est fourni à titre informatif uniquement et ne constitue pas un avis médical professionnel.
La vaccination initie une cascade moléculaire coordonnée couvrant la reconnaissance de motifs innés, le traitement et la présentation des antigènes, l’activation des lymphocytes, les réactions des centres germinatifs et l’établissement de la mémoire immunologique. Chaque étape implique des interactions récepteur-ligand distinctes, des voies de signalisation et des programmes de différenciation cellulaire. Ce qui suit est une description mécanistique de la façon dont les vaccins convertissent une rencontre antigénique transitoire en protection immunitaire durable.
Détection innée : récepteurs de reconnaissance de motifs et signaux de danger
La réponse immunitaire à la vaccination commence par la détection innée. Les récepteurs de type Toll (TLR), une famille de récepteurs de reconnaissance de motifs conservés du Caenorhabditis elegans aux mammifères, détectent les motifs moléculaires associés aux agents pathogènes (PAMP) présents dans les composants vaccinaux ou générés par eux. Les TLR sont des glycoprotéines membranaires intégrales de type I avec des domaines extracellulaires à répétitions riches en leucine et des domaines de signalisation cytoplasmiques d’homologie Toll/IL-1R (TIR).
Différents TLR reconnaissent des classes moléculaires distinctes. Les hétérodimères TLR1/2/6 détectent les lipopeptides bactériens. Le TLR4 (avec les co-récepteurs MD-2 et CD14) reconnaît le lipopolysaccharide. Le TLR3 détecte l’ARN double brin. Les TLR7/8 détectent l’ARN simple brin, et le TLR9 reconnaît les motifs CpG non méthylés. Les TLR de surface (1, 2, 4, 5, 6) détectent principalement les composants membranaires microbiens, tandis que les TLR endosomaux (3, 7, 8, 9) détectent les acides nucléiques qui nécessitent une internalisation pour la signalisation.
La signalisation TLR procède par deux grandes voies adaptatrices. La voie dépendante de MyD88 (utilisée par tous les TLR sauf TLR3) active les facteurs de transcription NF-kB et AP-1, stimulant la production de cytokines pro-inflammatoires (IL-6, TNF-alpha, IL-1bêta, IL-12). La voie dépendante de TRIF (TLR3 et TLR4) active IRF3, induisant des interférons de type I (IFN-alpha/bêta). Ces deux voies produisent des profils de cytokines différents qui façonnent l’immunité adaptative en aval : la signalisation MyD88 via les TLR de surface tend à favoriser la polarisation Th1 ou Th2, tandis que la signalisation TRIF-dépendante favorise les réponses Th1 et la présentation croisée aux lymphocytes T CD8+.
Au-delà des TLR, des capteurs cytoplasmiques contribuent également. RIG-I et MDA5 détectent l’ARN cytoplasmique, tandis que la voie cGAS-STING détecte l’ADN cytoplasmique. Pour les vaccins à ARNm spécifiquement, la réponse des lymphocytes T CD8+ au BNT162b2 s’est avérée dépendante de la signalisation MDA5 dépendante des interférons de type I, et non de la détection médiée par les TLR. La modification m1-pseudouridine dans l’ARNm du BNT162b2 atténue la reconnaissance par TLR3/7 et RIG-I tout en augmentant l’efficacité de traduction.
Les adjuvants comme amplificateurs de signal
Les adjuvants renforcent l’immunité adaptative en favorisant deux catégories de signaux des cellules présentatrices d’antigènes : le signal 1 (complexes peptide-CMH antigéniques) et le signal 2 (molécules co-stimulatrices CD40, CD80, CD86 et cytokines inflammatoires). Les sels d’aluminium, l’adjuvant le plus ancien homologué, favorisent la formation d’un dépôt antigénique et activent les cellules dendritiques inflammatoires par la libération d’acide urique des cellules nécrotiques. L’émulsion huile-dans-eau MF59, homologuée pour la première fois en Europe en 1997 après sept décennies de monopole des sels d’aluminium, recrute et active les CPA au site d’injection. L’AS03 (émulsion alpha-tocophérol + squalène) active la voie IRE1alpha/TRAF2/ASK1/JNK dans les cellules myéloïdes. L’AS04 combine l’hydroxyde d’aluminium avec l’agoniste TLR4 monophosphoryl lipide A (MPL).
Les vaccins à ARNm présentent une particularité : l’ARNm lui-même est intrinsèquement immunostimulant et est reconnu par de nombreux récepteurs de reconnaissance de motifs, permettant aux vaccins à ARNm d’induire des réponses robustes sans adjuvants supplémentaires. Le support nanoparticulaire lipidique contribue également à l’activité adjuvante par l’activation des voies de l’inflammasome et de NF-kB.
Traitement antigénique et présentation par le CMH
Les cellules dendritiques activées traitent les antigènes vaccinaux par deux grandes voies, chacune chargeant des peptides sur différentes molécules du CMH qui activent différentes populations de lymphocytes T.
Dans la voie exogène, les antigènes phagocytés sont dégradés dans les compartiments endosomaux/lysosomaux par les cathepsines et autres protéases. Les peptides résultants (typiquement 13 à 25 acides aminés) sont chargés sur les molécules du CMH de classe II et présentés aux lymphocytes T auxiliaires CD4+. C’est la voie dominante pour les vaccins à sous-unités protéiques et les vaccins inactivés.
Dans la voie endogène, les protéines synthétisées à l’intérieur de la cellule sont dégradées par le protéasome. Les peptides (typiquement 8 à 10 acides aminés) sont transportés dans le réticulum endoplasmique par le TAP (transporteur associé au traitement des antigènes), chargés sur les molécules du CMH de classe I et présentés aux lymphocytes T cytotoxiques CD8+. Cette voie est naturellement engagée lorsque les cellules sont infectées par un virus, et c’est pourquoi les vaccins à ARNm induisent efficacement des lymphocytes T cytotoxiques spécifiques à plusieurs épitopesRégion spécifique d'une molécule protéique reconnue par le système immunitaire comme cible. Dans la maladie cœliaque, certains épitopes des protéines du blé déclenchent une attaque immunitaire contre la paroi intestinale. par présentation endogène des antigènes : les ribosomes propres à la cellule traduisent l’ARNm en protéine, qui entre dans la voie de dégradation du protéasome.
Un troisième mécanisme, la présentation croisée, permet aux cellules dendritiques de charger des antigènes exogènes sur le CMH de classe I, activant ainsi les lymphocytes T CD8+ contre des menaces par lesquelles la cellule dendritique n’a pas elle-même été infectée. La présentation croisée se produit soit par une voie cytosolique (l’antigène s’échappe de l’endosome dans le cytosol pour le traitement par le protéasome) soit par une voie vacuolaire (le traitement a lieu dans les compartiments endocytiques). Ce mécanisme est essentiel pour les vaccins non réplicants qui doivent générer des réponses lymphocytaires T CD8+.
Activation des lymphocytes T : le modèle à trois signaux
L’activation d’un lymphocyte T naïf nécessite trois signaux coordonnés. Signal 1 : engagement du TCR avec le complexe peptide-CMH, assurant la spécificité antigénique. Signal 2 : liaison des récepteurs co-stimulateurs (CD28 sur les lymphocytes T se liant à CD80/CD86 sur les CPA), prévenant l’anergie. Signal 3 : polarisation médiée par les cytokines qui oriente la différenciation des lymphocytes T.
L’environnement cytokinique détermine le destin des lymphocytes T CD4+. L’IL-12 et l’IFN-gamma favorisent la polarisation Th1 (immunité à médiation cellulaire, commutation isotypique IgG2a). L’IL-4 favorise la polarisation Th2 (immunité humorale, commutation IgE/IgG1). L’IL-6 et le TGF-bêta favorisent la différenciation Th17. L’IL-6 et l’IL-21 favorisent la différenciation des cellules T auxiliaires folliculaires (Tfh), cruciale pour les réactions des centres germinatifs.
L’activation des lymphocytes T CD8+ suit les mêmes trois signaux requis, mais avec le CMH de classe I fournissant le signal 1. Les lymphocytes T CD8+ activés se différencient en lymphocytes T cytotoxiques (CTL) qui tuent les cellules cibles par apoptose médiée par la perforine/granzyme. La vaccination par BNT162b2 a produit une augmentation frappante des lymphocytes T CD8+ spécifiques à l’antigène après immunisation secondaire, avec une médiane de 10 % de lymphocytes T CD8+ positifs au tétramère CMH-I dans le poumon au jour 42. La réponse CD4+ était principalement polarisée Th1, avec une induction minimale d’IL-4.
La réaction des centres germinatifs : maturation d’affinité à résolution moléculaire
Le centre germinatif (CG) est la structure où les réponses lymphocytaires B sont affinées d’une reconnaissance large et de faible affinité vers un ciblage précis de haute affinité. Les lymphocytes B dans le CG se disputent des signaux dérivés des lymphocytes T limités, notamment des cytokines et le ligand CD40, qui favorisent leur migration entre la zone claire et la zone sombre.
Le CG a une architecture spatiale définie. Dans la zone sombre, les lymphocytes B (centroblastes) subissent une expansion clonale rapide et l’hypermutation somatiqueProcessus par lequel les lymphocytes B mutent rapidement leurs gènes d'anticorps pour affiner leur précision et leur affinité. (HMS) de leurs gènes de région variable des immunoglobulines. La désaminase cytidine induite par activation (AID) introduit des mutations ponctuelles à un taux d’environ 10^-3 par paire de bases par division, environ un million de fois supérieur au taux de mutation de fond.
Les lymphocytes B mutés migrent ensuite vers la zone claire, où ils testent leurs nouveaux récepteurs contre les antigènes affichés sur les cellules dendritiques folliculaires (CDF). Les lymphocytes B avec des récepteurs de plus haute affinité capturent et endocytent plus d’antigènes, présentant plus de complexes peptide-CMH II aux cellules Tfh. Cette densité plus élevée de peptide-CMH leur donne un avantage compétitif pour l’aide des lymphocytes T, médiée par une boucle de rétroaction positive de la signalisation CD40:CD40L.
Cette sélection compétitive produit deux destins divergents. Les lymphocytes B de haute affinité recevant de forts signaux Tfh régulent à la baisse Bcl-6 et régulent à la hausse IRF-4/Blimp-1, s’engageant dans la différenciation en plasmocytes. Les lymphocytes B de moindre affinité qui reçoivent une aide lymphocytaire T plus faible maintiennent l’expression de Bach2 et se différencient en lymphocytes B mémoire. Cette configuration contre-intuitive, où les lymphocytes B mémoire ont tendance à émerger du CG avant les plasmocytes et portent moins de mutations somatiques, garantit que le compartiment mémoire conserve amplitude et flexibilité, tandis que les plasmocytes assurent la précision.
La réponse des lymphocytes B des CG peut persister dans les ganglions lymphatiques drainants pendant au moins six mois chez certaines personnes après vaccination à ARNm, continuant à produire des cellules de sortie affinées longtemps après que l’antigène lui-même a été éliminé.
Mémoire immunologique : architecture de la protection à long terme
La protection vaccinale durable dépend de trois populations de mémoire distinctes, chacune opérant sur des échelles temporelles différentes et par des mécanismes différents.
Plasmocytes à longue durée de vie
Les plasmocytes à longue durée de vie (LLPC) persistent dans la moelle osseuse pendant des décennies en l’absence d’antigène, sécrétant continuellement des anticorps dans le sang. Leur survie dépend de facteurs de niche produits par les cellules stromales, les éosinophiles et les macrophages dans le microenvironnement de la moelle osseuse. Les LLPC fournissent la première ligne de défense humorale : des anticorps circulants préformés qui peuvent neutraliser un agent pathogène avant qu’il n’établisse l’infection.
Lymphocytes B mémoire
Les lymphocytes B mémoire augmentent en fréquence de 10 à 100 fois après le priming et produisent des anticorps d’affinité moyenne plus élevée que les lymphocytes B naïfs. Ils expriment des niveaux plus élevés de CMH de classe II, facilitant la capture et la présentation des antigènes à de faibles concentrations. En cas de réexposition, les lymphocytes B mémoire peuvent soit se différencier rapidement en cellules sécrétant des anticorps (fournissant une protection humorale rapide en deux à quatre jours plutôt que les deux semaines requises pour une réponse primaire) soit retourner dans les centres germinatifs pour une maturation d’affinité supplémentaire.
La capacité de réintégrer les CG est immunologiquement significative. Elle signifie que la vaccination de rappel ne fait pas que multiplier la mémoire existante, mais l’améliore activement, avec une affinité des anticorps continuant d’augmenter à chaque immunisation successive à mesure que les lymphocytes B mémoire subissent de nouveaux cycles d’hypermutation somatique et de sélection.
Lymphocytes T mémoire
Après la résolution de la phase effectrice, les lymphocytes T spécifiques à l’antigène persistent à des fréquences 100 à 1 000 fois supérieures aux fréquences pré-immunisation pour le reste de la vie de l’hôte. Les lymphocytes T mémoire se divisent en sous-ensembles fonctionnels : les lymphocytes T mémoire centraux (Tcm, CD62L+CCR7+) recirculent à travers les ganglions lymphatiques et prolifèrent rapidement lors d’une nouvelle rencontre ; les lymphocytes T mémoire effecteurs (Tem, CD62L-CCR7-) patrouillent les tissus périphériques et montent des réponses cytokiniques immédiates ; et les lymphocytes T mémoire résidents dans les tissus (Trm, CD69+CD103+) restent stationnés dans les tissus barrières comme le poumon et la muqueuse intestinale.
Cette architecture en couches, anticorps préformés par les LLPC, rappel rapide des lymphocytes B et lymphocytes T stationnés dans les tissus, fournit des systèmes de défense redondants qui rendent collectivement la réinfection beaucoup moins susceptible de provoquer une maladie grave.
Vaccins à ARNm : ingénierie de la voie endogène
Le lipide ionisable est le composant fonctionnel critique. Au pH physiologique (~7,4), il porte une charge neutre, permettant une pharmacocinétique favorable. Dans l’environnement endosomal acide (~pH 5-6), il devient protoné, interagissant avec la membrane endosomale anionique pour favoriser la formation d’une phase hexagonale et la libération du chargement dans le cytoplasme.
Une fois dans le cytoplasme, l’ARNm est traduit par les ribosomes de l’hôte en l’antigène encodé. Pour le BNT162b2, l’ARNm incorpore des modifications N1-méthylpseudouridine (m1-psi) qui atténuent les réponses inflammatoires médiées par TLR3/7 et RIG-I tout en augmentant l’efficacité de traduction et la stabilité biologique. La protéine spike exprimée entre dans la voie de présentation endogène du CMH de classe I (protéasome, TAP, chargement en RE) tout en étant sécrétée et absorbée par les CPA voisines pour la présentation du CMH de classe II et la présentation croisée.
Cette double présentation explique l’étendue de la réponse immunitaire : le BNT162b2 a induit à la fois de robustes réponses des lymphocytes B des centres germinatifs et des cellules Tfh et de puissantes réponses des lymphocytes T CD8+, la réponse immunitaire innée à la deuxième dose étant nettement plus forte qu’à la première, caractérisée par une production accrue d’IFN-gamma des cellules tueuses naturelles et des lymphocytes T CD8+ dans les ganglions lymphatiques drainants.
Immunité entraînéeCapacité des cellules immunitaires innées à répondre plus efficacement à de futures infections après une exposition antérieure, sans mémoire classique par anticorps. : reprogrammation épigénétique des cellules innées
La mémoire immunologique classique est une propriété du système immunitaire adaptatif. Cependant, un nombre croissant de preuves montre que les cellules immunitaires innées peuvent également développer une forme de mémoire. L’immunité entraînée implique une reprogrammation épigénétique et métabolique durable des cellules immunitaires innées telles que les monocytes et les macrophages, entraînant une réactivité renforcée aux infections ultérieures non apparentées.
Le vaccin BCG est l’exemple canonique. La vaccination induit des changements dans les modifications des histones (notamment les marques H3K4me3 et H3K27ac aux promoteurs des gènes inflammatoires) et des changements dans le métabolisme cellulaire (glycolyse accrue, activité altérée de la voie du mévalonate) qui persistent des mois, voire des années. Ces changements se propagent à travers les cellules progénitrices hématopoïétiques dans la moelle osseuse, fournissant un mécanisme à leur longévité malgré la durée de vie relativement courte des monocytes individuels.
L’immunité entraînée est mécanistiquement distincte de la mémoire adaptative : elle ne présente pas de spécificité antigénique, n’implique ni sélection clonale ni réarrangement des récepteurs, et fonctionne par remodelage de la chromatine plutôt que par recombinaison génique. Sa contribution à la protection médiée par les vaccins, notamment les effets hétérologues observés avec le BCG et d’autres vaccins vivants, représente un domaine d’investigation active aux implications potentielles pour la conception des vaccins.
Échappement aux variants et le problème de durabilité
L’immunité médiée par les anticorps est vulnérable à la dérive antigénique. Lorsqu’un agent pathogène mute ses protéines de surface, les anticorps préexistants peuvent ne plus se lier. C’est pourquoi les vaccins contre la grippe nécessitent une reformulation annuelle et pourquoi les variants du SRAS-CoV-2 portant des mutations dans la protéine spike ont montré une neutralisation réduite par les sérums vaccinaux.
L’immunité lymphocytaire T, cependant, est plus résiliente. Le balayage pangénomique des épitopes lymphocytaires T montre qu’environ 60 % des réponses des lymphocytes T CD8+ ciblent des protéines non structurales telles que ORF1ab, des régions conservées dans plus de 85 % du variant Omicron. Parce que les lymphocytes T reconnaissent des fragments de protéines intracellulaires (traités par le protéasome) plutôt que des conformations de surface, ils scrutent un ensemble beaucoup plus large de protéines virales, dont beaucoup sont soumises à des contraintes fonctionnelles plus fortes et mutent moins aisément.
Cette vulnérabilité bifurquée, où les anticorps sont spécifiques à une souche mais les lymphocytes T sont largement réactifs, explique une observation épidémiologique cohérente : les individus vaccinés peuvent être infectés par de nouveaux variants, mais ils sont nettement moins susceptibles de développer une maladie grave. Le mur des anticorps peut être percé, mais la défense cellulaire tient.
Cet article est fourni à titre informatif uniquement et ne constitue pas un avis médical professionnel.