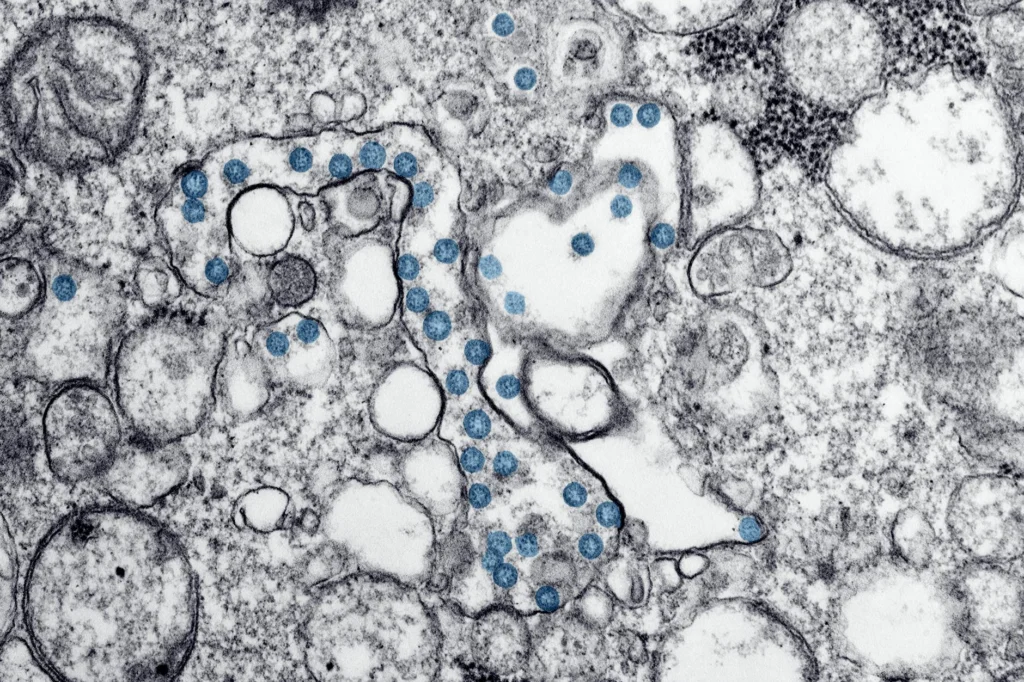
Jeder Impfstoff beruht auf derselben grundlegenden Täuschung: Er überzeugt Ihr Immunsystem, dass ein gefährlicher Erreger eingetroffen ist, ohne die eigentliche Gefahr. Was danach folgt, ist einer der ausgefeiltesten biologischen Prozesse im menschlichen Körper: eine mehrstufige Trainingsübung, die Ihre Abwehrkräfte dauerhaft gegen eine Bedrohung stärkt, der sie möglicherweise nie wirklich begegnet sind.
Diesen Mechanismus zu verstehen, geht über akademische Neugier hinaus. Im Zeitalter der mRNA-Impfstoffe, der Debatten über Pandemivorsorge und der wachsenden Fragen zu Auffrischungsimpfplänen ist die molekulare Maschinerie hinter der erworbenen Immunität nicht mehr nur Immunologie. Sie ist öffentliche Infrastruktur.
Der erste Alarm: Wie Ihr Körper einen Impfstoff erkennt
Wenige Minuten nach der Injektion erkennt Ihr angeborenes Immunsystem, der ältere und weniger spezifische Zweig der Immunität, den Impfstoff über Mustererkennungsrezeptoren (PRR). Diese Rezeptoren, insbesondere die Familie der Toll-like-Rezeptoren (TLR), suchen nach molekularen Signaturen, die mit Krankheitserregern assoziiert sind: fremde Proteine, Lipide oder Nukleinsäuren, die in gesundem Gewebe nichts verloren haben.
Dies ist keine gezielte Reaktion. Das angeborene Immunsystem weiß nicht, welcher spezifische Erreger eingetroffen ist. Es erkennt lediglich, dass etwas Fremdes vorhanden ist, und schlägt Alarm. Immunzellen an der Injektionsstelle, insbesondere dendritische Zellen und Makrophagen, beginnen, die Impfstoffkomponenten aufzunehmen. Sie zerlegen die Proteine in kleine Fragmente, sogenannte Peptide, und präsentieren diese auf ihrer Oberfläche mithilfe von Molekülen, dem MHC (Haupthistokompatibilitätskomplex).
Man kann sich das wie ein „Steckbriefplakat”-System vorstellen. Dendritische Zellen transportieren diese molekularen Steckbriefe von der Injektionsstelle zum nächsten Lymphknoten, wo das eigentliche Training beginnt.
Die Übergabe: Vom angeborenen zum adaptiven Immunsystem
Im Lymphknoten treffen angeborenes und adaptives Immunsystem aufeinander. Dendritische Zellen präsentieren ihre MHC-gebundenen Peptidfragmente den T-Zellen, spezialisierten weißen Blutkörperchen, die außerordentlich spezifische molekulare Formen erkennen können. Jede T-Zelle trägt einen einzigartigen Rezeptor auf ihrer Oberfläche, und von den Milliarden T-Zellen in Ihrem Körper werden nur wenige zum präsentierten Peptid passen.
Trifft eine Übereinstimmung ein, aktiviert sich diese T-Zelle. Sie beginnt sich schnell zu teilen und produziert eine Armee identischer Zellen. Einige werden zu „Helfer”-T-Zellen (CD4+), die die breitere Immunantwort koordinieren. Andere werden zu „Killer”-T-Zellen (CD8+), die Zellen mit dem Fremdprotein direkt zerstören können.
Helfer-T-Zellen sind besonders wichtig, weil sie B-Zellen aktivieren, einen anderen Typ von Immunzellen, der Antikörper produziert. Ohne die Signale der Helfer-T-Zellen können die meisten B-Zellen keine robuste Antikörperantwort aufbauen. Diese Zusammenarbeit zwischen Zelltypen erklärt, warum Adjuvanzien in Impfstoffen wirken, indem sie sowohl die Antigenpräsentation als auch die kostimulatorischen Signale verstärken, die diese Zell-zu-Zell-Kommunikation stärken.
Die Antikörperfabrik: B-Zellen und Keimzentren
Nach der Aktivierung durch Helfer-T-Zellen durchlaufen B-Zellen einen der bemerkenswertesten Prozesse der Biologie. Sie wandern zu spezialisierten Strukturen im Lymphknoten, den sogenannten Keimzentren, wo sie in einen Zyklus rascher Mutationen und Selektion eintreten, der Evolution im Zeitraffer nachahmt.
Im KeimzentrumSpezialisierte Struktur in Lymphknoten, in der B-Zellen nach einer Impfung Mutationen und Selektion durchlaufen, um hochaffine Antikörper zu bilden. teilen sich B-Zellen rasch, während sie zufällige Mutationen in die Gene einführen, die ihre Antikörperrezeptoren kodieren. Dieser Prozess, somatische HypermutationProzess, bei dem B-Zellen ihre Antikörpergene rasch mutieren, um Antikörper mit zunehmend höherer Affinität und Präzision zu erzeugen. genannt, ist kontrolliertes Chaos. Die meisten Mutationen sind nutzlos oder sogar schädlich. Aber einige produzieren Antikörper, die ihr Ziel stärker binden als zuvor.
B-Zellen mit verbesserten Antikörpern erhalten Überlebenssignale von Helfer-T-Zellen. Jene mit schwächeren Antikörpern erhalten keine und sterben ab. Im Laufe von Tagen und Wochen produziert dieser darwinistische Selektionsprozess Antikörper von zunehmend hoher Qualität. Deshalb sind die Antikörper, die Ihr Körper nach einer Auffrischungsimpfung bildet, typischerweise wirksamer als jene nach der ersten Dosis: Sie wurden durch mehrere Runden von Mutation und Selektion verfeinert.
Das Immungedächtnis: Der eigentliche Zweck
Das eigentliche Ergebnis einer Impfung ist nicht die anfängliche Immunantwort. Es ist das Gedächtnis. Nachdem die Impfstoffkomponenten beseitigt sind und die akute Reaktion abklingt, bleiben zwei Populationen langlebiger Zellen zurück.
Gedächtnis-B-Zellen sind Wächter, die jahrelang bis jahrzehntelang bestehen können. Wenn sie demselben Erreger erneut begegnen, differenzieren sie sich rasch in antikörperproduzierende Zellen und erzeugen eine schnellere und stärkere Antwort als beim ersten Mal. Während eine primäre Immunantwort etwa zwei Wochen benötigt, um nachweisbare Antikörper zu produzieren, erzeugt eine Gedächtnisantwort diese in nur zwei bis vier Tagen.
Gedächtnis-T-Zellen funktionieren ähnlich. Nach der Erstaktivierung sinkt die Zahl erregerspezifischer T-Zellen stark ab, stabilisiert sich jedoch auf einem Niveau, das 100- bis 1.000-mal höher liegt als vor der Impfung, und bleibt lebenslang bestehen. Diese Zellen sind nicht nur zahlreicher. Sie sind vorgerüstet, benötigen weniger Stimulation zur Reaktivierung und können eine Reaktion einleiten, bevor der Erreger Fuß fassen kann.
Langlebige Plasmazellen fügen eine dritte Schutzschicht hinzu. Diese Zellen, die hauptsächlich im Knochenmark ansässig sind, sezernieren kontinuierlich niedrige Antikörperspiegel über Jahrzehnte, auch ohne erneute Antigenexposition. Deshalb kann eine einzige Masernimpfung im Kindesalter lebenslangen Schutz bieten.
Warum Auffrischungsimpfungen wirken
Eine Auffrischungsdosis reaktiviert die Gedächtniszellen, die durch frühere Impfungen erzeugt wurden. Gedächtnis-B-Zellen treten erneut in Keimzentren ein und durchlaufen weitere Runden von Mutation und Selektion, wodurch die Antikörperaffinität mit jeder weiteren Immunisierung weiter steigt. Das Ergebnis sind Antikörper, die nicht nur häufiger vorkommen, sondern den Erreger auch besser neutralisieren.
Auffrischungsimpfungen erweitern auch die Gedächtnis-T-Zell-Population. Forschungen zu mRNA-COVID-19-Impfstoffen zeigten, dass die Sekundärimmunisierung eine bemerkenswerte Zunahme antigenspezifischer CD8+-T-Zellen bewirkte, insbesondere in den Lungen, einem der wichtigsten Orte für Atemwegsinfektionen.
Die mRNA-Revolution
Traditionelle Impfstoffe verwenden abgeschwächte oder inaktivierte Erreger oder gereinigte Proteine, um eine Immunantwort auszulösen. mRNA-Impfstoffe verfolgen einen grundlegend anderen Ansatz. Anstatt ein vorgefertigtes Antigen zu liefern, übermitteln sie genetische Anweisungen, verpackt in Lipid-Nanopartikeln aus vier Lipidkomponenten: ionisierbaren Lipiden, Hilfslipiden, Cholesterin und PEG-konjugierten Lipiden.
Einmal in einer Zelle angekommen, wird die mRNA durch die zelleigene Proteinsynthesemaschinerie in das Zielantigen übersetzt (bei COVID-19-Impfstoffen das Spike-Protein). Da das Protein innerhalb der Zelle produziert und nicht von außen zugeführt wird, wird es über denselben Weg verarbeitet, den der Körper für virusinfizierte Zellen nutzt. Das bedeutet, es wird auf MHC-Klasse-I-Molekülen präsentiert, was Killer-T-Zellen zusätzlich zur Antikörperantwort stark aktiviert.
Dies ist ein entscheidender Vorteil. mRNA-Impfstoffe induzieren durch endogene Antigenpräsentation effizient sowohl zytotoxische T-Zellen als auch gewebsständige Gedächtnis-T-Zellen, was mit traditionellen inaktivierten Impfstoffen schwieriger zu erreichen ist.
Jenseits des Individualschutzes: Trainierte ImmunitätFähigkeit angeborener Immunzellen, nach einer Voraktivierung auf künftige Infektionen wirksamer zu reagieren, ohne auf klassisches Gedächtnis durch Antikörper zurückzugreifen.
Eine der überraschendsten Erkenntnisse der modernen Immunologie ist, dass einige Impfstoffe offenbar auch das angeborene Immunsystem trainieren, nicht nur den adaptiven Arm. Dieses Phänomen, trainierte Immunität genannt, umfasst dauerhafte Veränderungen der angeborenen Immunzellen durch epigenetische und metabolische Umprogrammierung.
Der BCG-Impfstoff (gegen Tuberkulose) ist das am meisten untersuchte Beispiel. Mit BCG geimpfte Personen zeigen eine verstärkte Resistenz nicht nur gegen Tuberkulose, sondern auch gegen unverwandte Infektionen, was darauf hindeutet, dass der Impfstoff ein umfassend wachsameres angeborenes Immunsystem induziert. Dies ist kein klassisches immunologisches Gedächtnis. Es funktioniert über völlig andere Mechanismen und verändert, wie Gene in angeborenen Immunzellen abgelesen werden, ohne die DNA-Sequenz selbst zu verändern.
Was schiefgehen kann
Kein System dieser Komplexität funktioniert jedes Mal perfekt. Manche Menschen erzeugen aufgrund von Alter, Immunsuppression oder genetischer Variation schwächere Immunantworten. Ältere Menschen neigen insbesondere dazu, weniger Keimzentrumsreaktionen zu produzieren und Antikörper von geringerer Qualität zu bilden, weshalb Impfformulierungen für ältere Erwachsene häufig stärkere Adjuvanzien enthalten.
Erreger können sich auch weiterentwickeln, um dem Immungedächtnis zu entkommen. Influenza mutiert seine Oberflächenproteine so schnell, dass Antikörper vom Vorjahr den diesjährigen Stamm möglicherweise nicht erkennen. SARS-CoV-2-Varianten mit Mutationen im Spike-Protein können den Antikörpern, die gegen frühere Stämme gebildet wurden, teilweise entkommen. Allerdings erhalten T-Zellen, die auf konservierte Virusregionen abzielen, ihre Erkennungsfähigkeit über Varianten hinweg, weshalb geimpfte Personen weiterhin weitgehend gegen schwere Erkrankungen geschützt sind, selbst wenn die Antikörperwirksamkeit nachlässt.
Dies ist ein entscheidender Punkt, der in öffentlichen Debatten oft untergeht: Antikörper sind nicht das einzige Maß für den Impfschutz. Die T-Zell-Immunität bildet eine dauerhafte zweite Verteidigungslinie, die Erregern schwerer zu überwinden fällt.
Dieser Artikel dient ausschließlich Informationszwecken und stellt keine professionelle medizinische Beratung dar.
Die Impfung initiiert eine koordinierte molekulare Kaskade, die angeborene Mustererkennung, Antigenverarbeitung und -präsentation, Lymphozytenaktivierung, Keimzentrumsreaktionen und die Etablierung eines immunologischen Gedächtnisses umfasst. Jede Phase beinhaltet spezifische Rezeptor-Ligand-Wechselwirkungen, Signalwege und zelluläre Differenzierungsprogramme. Im Folgenden wird mechanistisch beschrieben, wie Impfstoffe eine vorübergehende Antigenexposition in dauerhaften Immunschutz umwandeln.
Angeborene Erkennung: Mustererkennungsrezeptoren und Gefahrensignale
Die Immunantwort auf eine Impfung beginnt mit der angeborenen Erkennung. Toll-like-Rezeptoren (TLR), eine Familie von Mustererkennungsrezeptoren, die von Caenorhabditis elegans bis zu Säugetieren konserviert sind, erkennen pathogenassoziierte molekulare Muster (PAMP), die in Impfstoffkomponenten vorhanden sind oder von ihnen erzeugt werden. TLRs sind integrale Typ-I-Membranglykoproteine mit leucinreichen extrazellulären Wiederholungsdomänen und zytoplasmatischen Toll/IL-1R (TIR)-Homologiesignaldomänen.
Verschiedene TLRs erkennen unterschiedliche Molekülklassen. TLR1/2/6-Heterodimere detektieren bakterielle Lipopeptide. TLR4 (mit den Ko-Rezeptoren MD-2 und CD14) erkennt Lipopolysaccharid. TLR3 detektiert doppelsträngige RNA. TLR7/8 erfasst einzelsträngige RNA, und TLR9 erkennt unmethylierte CpG-DNA-Motive. Oberflächen-TLRs (1, 2, 4, 5, 6) detektieren vorwiegend mikrobielle Membrankomponenten, während endosomale TLRs (3, 7, 8, 9) Nukleinsäuren erkennen, die zur Signalübertragung internalisiert werden müssen.
Die TLR-Signalgebung verläuft über zwei Hauptadaptor-Wege. Der MyD88-abhängige Weg (genutzt von allen TLRs außer TLR3) aktiviert die Transkriptionsfaktoren NF-kB und AP-1 und treibt die Produktion proinflammatorischer ZytokineKleine Signalproteine, die von Immunzellen freigesetzt werden und Entzündungsreaktionen koordinieren. Erhöhte Spiegel werden zuverlässig bei Depressionspatienten gefunden. (IL-6, TNF-alpha, IL-1beta, IL-12) an. Der TRIF-abhängige Weg (TLR3 und TLR4) aktiviert IRF3 und induziert Typ-I-Interferone (IFN-alpha/beta). Diese beiden Wege erzeugen unterschiedliche Zytokinprofile, die die nachgeschaltete adaptive Immunität prägen: MyD88-Signalgebung über Oberflächen-TLRs tendiert zur Th1- oder Th2-Polarisierung, während TRIF-abhängige Signalgebung Th1-Antworten und Kreuzpräsentation auf CD8+-T-Zellen fördert.
Über TLRs hinaus tragen auch zytoplasmatische Sensoren bei. RIG-I und MDA5 detektieren zytoplasmatische RNA, während der cGAS-STING-Weg zytoplasmatische DNA erfasst. Speziell bei mRNA-Impfstoffen erwies sich die CD8+-T-Zell-Antwort auf BNT162b2 als abhängig von Typ-I-Interferon-abhängiger MDA5-Signalgebung, nicht von TLR-vermittelter Erkennung. Die m1-PseudouridinEine chemisch modifizierte Form von Uridin, einem der vier RNA-Bausteine. Sein Einbau in synthetische mRNA verhindert, dass das Immunsystem die mRNA vorzeitig abbaut.-Modifikation in der BNT162b2-mRNA dämpft die TLR3/7- und RIG-I-Erkennung, erhöht dabei aber die Translationseffizienz.
Adjuvanzien als Signalverstärker
Adjuvanzien steigern die adaptive Immunität, indem sie zwei Kategorien von Signalen der antigenpräsentierenden Zellen fördern: Signal 1 (Antigen-Peptid-MHC-Komplexe) und Signal 2 (kostimulatorische Moleküle CD40, CD80, CD86 sowie entzündliche Zytokine). Aluminiumsalze, das älteste zugelassene AdjuvansHilfsstoff, der Impfstoffen zugesetzt wird, um die Immunantwort zu verstärken, ohne selbst das Zielantigen zu sein., fördern die Antigendepotbildung und aktivieren inflammatorische dendritische Zellen durch Freisetzung von Harnsäure aus nekrotischen Zellen. Die Öl-in-Wasser-Emulsion MF59, erstmals 1997 in Europa zugelassen nach sieben Jahrzehnten des Aluminiumsalz-Monopols, rekrutiert und aktiviert APCs an der Injektionsstelle. AS03 (Alpha-Tocopherol-Squalen-Emulsion) aktiviert den IRE1alpha/TRAF2/ASK1/JNK-Signalweg in myeloiden Zellen. AS04 kombiniert Aluminiumhydroxid mit dem TLR4-Agonisten Monophosphoryl-Lipid A (MPL).
mRNA-Impfstoffe haben die Besonderheit, dass die mRNA selbst inhärent immunstimulierend ist und von zahlreichen Mustererkennungsrezeptoren erkannt wird, sodass mRNA-basierte Impfstoffe robuste Antworten ohne zusätzliche Adjuvanzien induzieren können. Der Lipid-Nanopartikel-Träger trägt ebenfalls zur Adjuvanzwirkung bei, indem er Inflammasom- und NF-kB-Wege aktiviert.
Antigenverarbeitung und MHC-Präsentation
Aktivierte dendritische Zellen verarbeiten Impfstoffantigene über zwei Hauptwege, wobei jeder Peptide auf unterschiedliche MHC-Moleküle lädt, die verschiedene T-Zell-Populationen aktivieren.
Im exogenen Weg werden phagozytierte Antigene in endosomalen/lysosomalen Kompartimenten durch Cathepsine und andere Proteasen abgebaut. Die resultierenden Peptide (typischerweise 13 bis 25 Aminosäuren) werden auf MHC-Klasse-II-Moleküle geladen und CD4+-Helfer-T-Zellen präsentiert. Dies ist der dominante Weg für Proteinuntereinheits- und inaktivierte Impfstoffe.
Im endogenen Weg werden in der Zelle synthetisierte Proteine durch das Proteasom abgebaut. Peptide (typischerweise 8 bis 10 Aminosäuren) werden durch TAP (Transportprotein assoziiert mit Antigenverarbeitung) ins endoplasmatische Retikulum transportiert, auf MHC-Klasse-I-Moleküle geladen und CD8+-zytotoxischen T-Zellen präsentiert. Dieser Weg wird natürlich aktiviert, wenn Zellen durch ein Virus infiziert werden, und erklärt, warum mRNA-Impfstoffe durch endogene Antigenpräsentation effizient multiepitopspezifische zytotoxische T-Lymphozyten induzieren: Die zelleigenen Ribosomen übersetzen die mRNA in ein Protein, das in den Proteasom-Abbauweg eingeht.
Ein dritter Mechanismus, die Kreuzpräsentation, ermöglicht dendritischen Zellen, exogene Antigene auf MHC-Klasse-I zu laden und so CD8+-T-Zellen gegen Bedrohungen zu aktivieren, mit denen die dendritische Zelle selbst nicht infiziert wurde. Die Kreuzpräsentation erfolgt entweder über einen zytosolischen Weg (das Antigen entkommt dem Endosom ins Zytosol zur Proteasom-Verarbeitung) oder einen vakuolären Weg (die Verarbeitung findet in endozytischen Kompartimenten statt). Dieser Mechanismus ist entscheidend für nicht replizierende Impfstoffe, die CD8+-T-Zell-Antworten erzeugen müssen.
T-Zell-Aktivierung: Das Drei-Signal-Modell
Die Aktivierung naiver T-Zellen erfordert drei koordinierte Signale. Signal 1: TCR-Bindung an den Peptid-MHC-Komplex, die Antigenspezifität bereitstellend. Signal 2: Bindung des kostimulatorischen Rezeptors (CD28 auf T-Zellen bindet an CD80/CD86 auf APCs) zur Verhinderung von Anergie. Signal 3: zytokinvermittelte Polarisierung, die die T-Zell-Differenzierung lenkt.
Das Zytokinmilieu bestimmt das Schicksal von CD4+-T-Zellen. IL-12 und IFN-gamma treiben Th1-Polarisierung an (zellvermittelte Immunität, IgG2a-Isotypenumschaltung). IL-4 treibt Th2-Polarisierung an (humorale Immunität, IgE/IgG1-Umschaltung). IL-6 und TGF-beta fördern Th17-Differenzierung. IL-6 und IL-21 fördern die Differenzierung follikulärer Helfer-T-Zellen (Tfh), was für Keimzentrumsreaktionen entscheidend ist.
Die CD8+-T-Zell-Aktivierung folgt denselben drei Signalvoraussetzungen, wobei MHC-Klasse-I Signal 1 bereitstellt. Aktivierte CD8+-T-Zellen differenzieren zu zytotoxischen T-Lymphozyten (CTL), die Zielzellen durch Perforin/Granzym-vermittelte Apoptose töten. Die BNT162b2-Impfung erzeugte nach Sekundärimmunisierung eine bemerkenswerte Zunahme antigenspezifischer CD8+-T-Zellen, mit einem Median von 10 % MHC-I-Tetramer-positiver CD8+-T-Zellen in der Lunge an Tag 42. Die CD4+-Antwort war vorwiegend Th1-polarisiert, mit minimaler IL-4-Induktion.
Die Keimzentrumsreaktion: Affinitätsreifung auf molekularer Ebene
Das KeimzentrumSpezialisierte Struktur in Lymphknoten, in der B-Zellen nach einer Impfung Mutationen und Selektion durchlaufen, um hochaffine Antikörper zu bilden. (GC) ist die Struktur, in der B-Zell-Antworten von breiter Erkennung mit geringer Affinität zu präzisem Targeting mit hoher Affinität verfeinert werden. B-Zellen im GC konkurrieren um begrenzte T-Zell-Signale, einschließlich Zytokinen und CD40-Ligand, die ihre Migration zwischen der Licht- und Dunkelzone fördern.
Das GC hat eine definierte räumliche Architektur. In der Dunkelzone durchlaufen B-Zellen (Zentroblasten) schnelle klonale Expansion und somatische HypermutationProzess, bei dem B-Zellen ihre Antikörpergene rasch mutieren, um Antikörper mit zunehmend höherer Affinität und Präzision zu erzeugen. (SHM) ihrer Immunglobulin-Variablenregion-Gene. Die aktivierungsinduzierte Cytidindesaminase (AID) führt Punktmutationen mit einer Rate von etwa 10^-3 pro Basenpaar pro Teilung ein, was rund eine Million Mal über der Hintergrundmutationsrate liegt.
Mutierte B-Zellen wandern dann in die Lichtzone, wo sie ihre neuen Rezeptoren gegen Antigene testen, die auf follikulären dendritischen Zellen (FDC) präsentiert werden. B-Zellen mit höheraffinitiven Rezeptoren nehmen mehr Antigen auf und endozytieren es, wobei sie mehr Peptid-MHC-II-Komplexe den Tfh-Zellen präsentieren. Diese höhere Peptid-MHC-Dichte verschafft ihnen einen Wettbewerbsvorteil bei der T-Zell-Hilfe, vermittelt durch eine positive Rückkopplungsschleife der CD40:CD40L-Signalgebung.
Diese kompetitive Selektion führt zu zwei abweichenden Schicksalen. Hochaffine B-Zellen, die starke Tfh-Signale erhalten, regulieren Bcl-6 herunter und IRF-4/Blimp-1 herauf, was sie zur Plasmazell-Differenzierung verpflichtet. B-Zellen mit geringerer Affinität, die schwächere T-Zell-Hilfe erhalten, behalten die Bach2-Expression bei und differenzieren zu Gedächtnis-B-Zellen. Diese kontraintuitive Anordnung, bei der Gedächtnis-B-Zellen tendenziell früher aus dem GC hervorgehen als Plasmazellen und weniger somatische Mutationen tragen, stellt sicher, dass das Gedächtniskompartiment Breite und Flexibilität behält, während Plasmazellen Präzision liefern.
Die GC-B-Zell-Antwort kann in drainierenden Lymphknoten bei einigen Personen nach mRNA-Impfung mindestens sechs Monate anhalten und produziert lang nach der Antigenbeseitigung weiterhin affinitätsgereifte Ausgangszellen.
Immunologisches Gedächtnis: Architektur des Langzeitschutzes
Dauerhafter Impfschutz hängt von drei verschiedenen Gedächtnispopulationen ab, die jeweils auf unterschiedlichen Zeitskalen und durch unterschiedliche Mechanismen operieren.
Langlebige Plasmazellen
Langlebige Plasmazellen (LLPC) persistieren jahrzehntelang im Knochenmark in Abwesenheit von Antigen und sezernieren kontinuierlich Antikörper in den Blutkreislauf. Ihr Überleben hängt von Nischenfaktoren ab, die von Stromazellen, Eosinophilen und Makrophagen in der Knochenmarkmikroumgebung produziert werden. LLPCs bilden die erste Linie der humoralen Abwehr: vorgeformte zirkulierende Antikörper, die einen Erreger neutralisieren können, bevor er eine Infektion etabliert.
Gedächtnis-B-Zellen
Gedächtnis-B-Zellen erhöhen ihre Häufigkeit nach dem Priming um das 10- bis 100-fache und produzieren Antikörper mit höherer Durchschnittsaffinität als naive B-Zellen. Sie exprimieren höhere MHC-Klasse-II-Spiegel, was Antigenaufnahme und -präsentation bei geringeren Antigenkonzentrationen erleichtert. Bei erneuter Exposition können Gedächtnis-B-Zellen entweder schnell in antikörpersezenierende Zellen differenzieren (was raschen humoralen Schutz in zwei bis vier Tagen statt der zwei Wochen einer Primärantwort bietet) oder erneut in Keimzentren eintreten für weitere Affinitätsreifung.
Die Fähigkeit, erneut in GCs einzutreten, ist immunologisch bedeutsam. Sie bedeutet, dass Auffrischungsimpfungen nicht einfach das bestehende Gedächtnis ausweiten, sondern es aktiv verbessern, wobei die Antikörperaffinität mit jeder weiteren Immunisierung weiter steigt, da Gedächtnis-B-Zellen weitere Runden somatischer Hypermutation und Selektion durchlaufen.
Gedächtnis-T-Zellen
Nach Abklingen der Effektorphase persistieren antigenspezifische T-Zellen bei 100- bis 1.000-fach höheren Frequenzen als vor der Immunisierung für den Rest des Lebens des Wirts. Gedächtnis-T-Zellen unterteilen sich in funktionelle Teilmengen: zentrale Gedächtnis-T-Zellen (Tcm, CD62L+CCR7+) zirkulieren durch Lymphknoten und proliferieren bei erneuter Begegnung rasch; Effektor-Gedächtnis-T-Zellen (Tem, CD62L-CCR7-) patrouillieren periphere Gewebe und initiieren unmittelbare Zytokinantworten; und gewebsständige Gedächtnis-T-Zellen (Trm, CD69+CD103+) bleiben in Barrierengeweben wie Lunge und Darmmukosa stationiert.
Diese Schichtarchitektur, vorgeformte Antikörper der LLPCs, schneller B-Zell-Recall und gewebsstationierte T-Zellen, liefert überlappende und redundante Abwehrsysteme, die kollektiv eine Reinfektion mit schwerem Krankheitsverlauf wesentlich unwahrscheinlicher machen.
mRNA-Impfstoffe: Nutzung des endogenen Wegs
Das ionisierbare Lipid ist die kritische funktionelle Komponente. Bei physiologischem pH (~7,4) trägt es eine neutrale Ladung, was günstige pharmakokinetische Eigenschaften ermöglicht. In der sauren endosomalen Umgebung (~pH 5-6) wird es protoniert, interagiert mit der anionischen endosomalen Membran zur Förderung der hexagonalen Phasenbildung und setzt die Fracht ins Zytoplasma frei.
Im Zytoplasma angekommen, wird die mRNA durch Wirtsribosomen in das kodierte Antigen translatiert. Für BNT162b2 enthält die mRNA N1-Methylpseudouridin (m1-psi)-Modifikationen, die TLR3/7- und RIG-I-vermittelte Entzündungsreaktionen dämpfen, während Translationseffizienz und biologische Stabilität erhöht werden. Das exprimierte Spike-Protein tritt in den endogenen MHC-Klasse-I-Präsentationsweg ein (Proteasom, TAP, ER-Beladung) und wird zugleich sezerniert und von benachbarten APCs für die MHC-Klasse-II-Präsentation und Kreuzpräsentation aufgenommen.
Diese duale Präsentation erklärt die Breite der Immunantwort: BNT162b2 induzierte sowohl robuste Keimzentrum-B-Zell- und Tfh-Antworten als auch potente CD8+-T-Zell-Antworten, wobei die angeborene Immunantwort auf die zweite Dosis deutlich stärker war als auf die erste, gekennzeichnet durch verstärkte IFN-gamma-Produktion aus natürlichen Killerzellen und CD8+-T-Zellen in drainierenden Lymphknoten.
Trainierte ImmunitätFähigkeit angeborener Immunzellen, nach einer Voraktivierung auf künftige Infektionen wirksamer zu reagieren, ohne auf klassisches Gedächtnis durch Antikörper zurückzugreifen.: Epigenetische Umprogrammierung angeborener Zellen
Das klassische immunologische Gedächtnis ist eine Eigenschaft des adaptiven Immunsystems. Eine wachsende Zahl von Belegen zeigt jedoch, dass auch angeborene Immunzellen eine Form von Gedächtnis entwickeln können. Trainierte Immunität umfasst dauerhafte epigenetische und metabolische Umprogrammierung angeborener Immunzellen wie Monozyten und Makrophagen, was zu verstärkter Reaktionsfähigkeit auf nachfolgende, nicht verwandte Infektionen führt.
Der BCG-Impfstoff ist das kanonische Beispiel. Die Impfung induziert Veränderungen in Histonmodifikationen (insbesondere H3K4me3- und H3K27ac-Markierungen an Promotoren entzündlicher Gene) und Verschiebungen im Zellstoffwechsel (erhöhte Glykolyse, veränderte Mevalonat-Stoffwechselaktivität), die monate- bis jahrelang anhalten. Diese Veränderungen werden über hämatopoetische Vorläuferzellen im Knochenmark weitergegeben, was einen Mechanismus für ihre Langlebigkeit trotz der relativ kurzen Lebensspanne einzelner Monozyten liefert.
Trainierte Immunität unterscheidet sich mechanistisch vom adaptiven Gedächtnis: Sie besitzt keine Antigenspezifität, beinhaltet weder klonale Selektion noch Rezeptorumordnung und operiert über Chromatinmodellierung statt Genrekombination. Ihr Beitrag zum impfvermittelten Schutz, insbesondere die bei BCG und anderen Lebendimpfstoffen beobachteten heterologen Effekte, ist ein aktives Forschungsfeld mit potenziellen Implikationen für die Impfstoffentwicklung.
Variantenflucht und das Dauerhaftigkeitsproblem
Antikörpervermittelte Immunität ist anfällig für antigene Drift. Wenn ein Erreger seine Oberflächenproteine mutiert, können vorhandene Antikörper möglicherweise nicht mehr binden. Deshalb müssen Influenzaimpfstoffe jährlich neu formuliert werden, und SARS-CoV-2-Varianten mit Spike-Protein-Mutationen zeigten eine verminderte Neutralisation durch impfinduzierte Seren.
Die T-Zell-Immunität ist jedoch widerstandsfähiger. Genomweites T-Zell-EpitopEine spezifische Region auf einem Proteinmolekül, die das Immunsystem als Angriffsziel erkennt. Bei Zöliakie lösen bestimmte Epitope auf Weizenproteinen einen Immunangriff auf die Darmwand aus.-Scanning zeigt, dass etwa 60 % der CD8+-T-Zell-Antworten auf nichtstrukturelle Proteine wie ORF1ab abzielen, Regionen, die in mehr als 85 % der Omicron-Variante konserviert sind. Da T-Zellen intrazelluläre Proteinfragmente erkennen (durch das Proteasom verarbeitet) statt Oberflächenkonformationen, überblicken sie einen viel breiteren Satz viraler Proteine, von denen viele unter stärkeren funktionellen Einschränkungen stehen und weniger leicht mutieren.
Diese bifurkierte Anfälligkeit, bei der Antikörper stammspezifisch, T-Zellen aber breit kreuzreaktiv sind, erklärt eine konsistente epidemiologische Beobachtung: Geimpfte können sich mit neuen Varianten infizieren, sind aber deutlich weniger anfällig für schwere Erkrankungen. Die Antikörpermauer kann durchbrochen werden, aber die zelluläre Abwehr hält stand.
Dieser Artikel dient ausschließlich Informationszwecken und stellt keine professionelle medizinische Beratung dar.