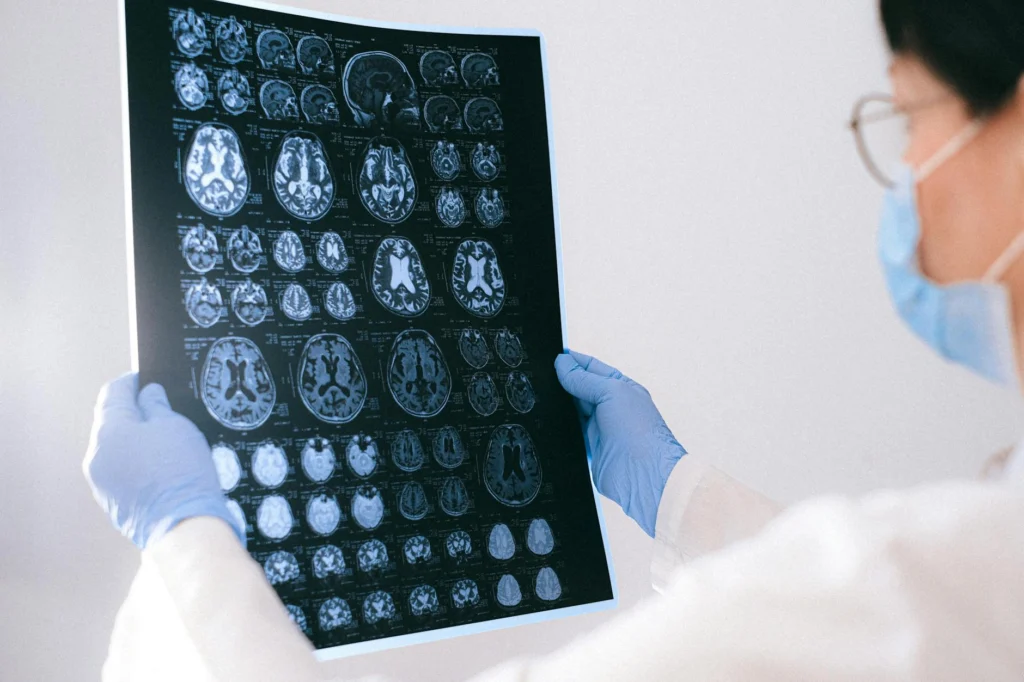
Mehr als 3 Milliarden Menschen weltweit leben mit einer neurologischen Erkrankung, was Hirnerkrankungen zur häufigsten Ursache von Krankheit und Behinderung auf der Welt macht. Dennoch bleibt die Medikamentenzufuhr durch die Blut-Hirn-SchrankeEine selektive Membran, die kontrolliert, welche Stoffe aus dem Blutkreislauf ins Gehirn gelangen. Nanoplastik ist klein genug, um diese Barriere zu durchqueren und sich in Gehirngewebe anzusammeln. der hartnäckigste EngpassEin geografischer Ort, an dem der Verkehr durch eine enge oder begrenzte Passage führen muss, was zu einer Anfälligkeit für Störungen führt. der Medizin: Rund 98 % der niedermolekularen Wirkstoffe erreichen niemals das Hirngewebe, das sie behandeln sollen. Diese Zahl ist kein Schätzfehler. Sie ist die grundlegende Einschränkung der Neuropharmakologie, und um zu verstehen, warum sie existiert, muss man sich eine biologische Struktur ansehen, die so effektiv ist, dass sie zu ihrer eigenen Feindin geworden ist.
Was die Blut-Hirn-Schranke tatsächlich ist
Erstmals von Paul Ehrlich im Jahr 1885 beschrieben, ist die Blut-Hirn-Schranke (BHS) keine Wand. Sie ist ein lebendiger, streng regulierter Filter, der in die Wände jeder Kapillare eingebaut ist, die das Gehirn versorgt. Die Kernstruktur besteht aus Endothelzellen, die durch Tight Junctions zusammengehalten werden, Proteinkomplexen, die die Lücken zwischen benachbarten Zellen so gründlich abdichten, dass nahezu nichts hindurchdringt.
In den meisten Körperbereichen sind Kapillaren relativ durchlässig. Sie haben kleine Poren, lockere Verbindungen und Lücken, durch die Moleküle frei zwischen Blut und Gewebe wechseln können. Gehirnkapillaren sind anders. Ihre Endothelzellen sind durch überlappende Reihen von Tight-Junction-Proteinen verbunden, vor allem Claudin-5 und Occludin, die eine nahezu durchgehende Dichtung bilden. Das Ergebnis ist messbar: Der elektrische Widerstand über Hirnkapillaren beträgt 1.500 bis 2.000 Ohm pro Quadratzentimeter, verglichen mit nur 3 bis 30 in peripheren Kapillaren. Das ist ein 50-facher Unterschied in der Dichtigkeit der Schranke.
Doch die Endothelzellen arbeiten nicht allein. Astrozytenendfüße umhüllen über 99 % der Gehirnkapillaren und liefern chemische Signale, die die Barrierefestigkeit aufrechterhalten. Perizyten, in die Kapillarwand eingebettete Zellen, kommen im Gehirn in einem Verhältnis von etwa einem Perizyten pro ein bis drei Endothelzellen vor, gegenüber einem pro hundert im Muskelgewebe. Gemeinsam bilden diese Zellen die neurovaskuläre EinheitMehrzelluläres System um Hirnkapillaren, bestehend aus Endothelzellen, Perizyten und Astrozyten, das die Blut-Hirn-Schranke bildet und aufrechterhält., ein mehrschichtiges Verteidigungssystem, das die chemische Umgebung des Gehirns außergewöhnlich stabil hält.
Medikamentenzufuhr durch die Blut-Hirn-Schranke: Warum Wirkstoffe nicht durchkommen
Die Schranke lässt passiv nur eine schmale Klasse von Molekülen passieren: fettlösliche Verbindungen mit einem Gewicht von weniger als etwa 400 bis 600 Dalton. Das umfasst einige nützliche Wirkstoffe (Alkohol, Koffein, bestimmte Anästhetika), schließt aber die überwiegende Mehrheit moderner Therapeutika aus, darunter Antikörper, Gentherapien und die meisten rekombinanten Proteine.
Selbst Wirkstoffe, die eigentlich funktionieren sollten, sehen sich einer zweiten Verteidigungslinie gegenüber: Effluxpumpen. P-GlykoproteinEine Proteinpumpe in den Wänden von Hirnkapillaren, die Wirkstoffe aktiv ins Blut zurückbefördert und so ihre Anreicherung im Hirngewebe verhindert., die am intensivsten erforschte dieser Pumpen, sitzt auf der blutseitigen Oberfläche der Endothelzellen und schleust aktiv ein breites Spektrum von Molekülen zurück in den Blutkreislauf. Ein Wirkstoff kann die Zellmembran überwinden, wird aber sofort wieder herausgepumpt, bevor er das Hirngewebe erreicht. Das ist keine Theorie. Bei der Epilepsie ist etwa ein Drittel der Patienten pharmakoresistent, und die Überexpression von P-Glykoprotein in epileptischen Hirnregionen gilt als wesentliche Ursache.
Die Konsequenzen für die Medikamentenentwicklung sind gravierend. Die Misserfolgsrate von ZNS-Wirkstoffen in Phase-2- und Phase-3-Studien liegt bei etwa 85 %, nur von der Onkologie übertroffen. Insgesamt erhalten nur 6,2 % der ZNS-Wirkstoffe eine klinische Zulassung, verglichen mit 13,3 % in anderen Therapiebereichen. Die Entwicklung von ZNS-Wirkstoffen dauert zudem fast 13 Monate länger. Viele große Pharmaunternehmen haben daraufhin das Feld vollständig verlassen.
Das Antikörper-Problem
Die moderne Medizin wurde durch monoklonale Antikörper revolutioniert. Sie behandeln Krebs, Autoimmunerkrankungen und Infektionen mit bemerkenswerter Präzision. Antikörper sind jedoch riesige Moleküle, typischerweise rund 150.000 Dalton, ungefähr 375-mal so groß wie das Größenlimit für die passive Diffusion durch die BHS. Weniger als 0,1 % der injizierten Antikörper erreichen das Gehirn.
Das erzeugt ein schmerzhaftes Paradox bei der Alzheimer-Krankheit. Lecanemab und Aducanumab, die Antikörper zur Beseitigung von Amyloidplaques, müssen in extrem hohen systemischen Dosen verabreicht werden, um überhaupt einen winzigen Bruchteil ins Gehirn zu befördern. Die Nebenwirkungen, darunter Hirnödeme und Mikroblutungen (zusammenfassend ARIA genannt), sind zum Teil eine Folge der massiven Dosierung, die nötig ist, um die Schranke zu überwinden. Das Medikament wirkt, aber das Zuleitungsproblem verwandelt eine gezielte Therapie in ein stumpfes Instrument.
Strategien, die erste Erfolge zeigen
Die vielversprechendsten Ansätze versuchen nicht, Wirkstoffe mit Gewalt durch die Schranke zu pressen. Sie nutzen die eigene Biologie der Schranke.
Rezeptorvermittelte TranszytoseProzess, bei dem Moleküle an Zelloberflächenrezeptoren binden und in Vesikeln durch die Zelle transportiert werden, um Wirkstoffe ins Gehirn zu schleusen.
Das Gehirn benötigt Eisen, Glukose und Insulin und verfügt daher über eingebaute Transportsysteme dafür. Die rezeptorvermittelte Transzytose nutzt diese natürlichen Wege, indem therapeutische Fracht an Moleküle gebunden wird, die die Rezeptoren der Schranke erkennen und hindurchtransportieren. Der Transferrinrezeptor, der Eisen importiert, ist das am häufigsten genutzte Ziel. Denali Therapeutics hat Antikörperfragmente entwickelt, die an den Transferrinrezeptor binden und das Transportsystem ins Gehirn nutzen, wobei sie therapeutische Proteine mitnehmen. Dieser Ansatz hat Phase-1-Studien für das Hunter-Syndrom und die frontotemporale Demenz erreicht.
Fokussierter Ultraschall
Statt sich an der Schranke vorbeizuschleichen, öffnet fokussierter Ultraschall sie vorübergehend. In den Blutkreislauf injizierte Mikrobläschen werden durch präzise ausgerichtete Ultraschallwellen in Schwingung versetzt und lockern mechanisch die Tight Junctions in einer gezielten Hirnregion für einige Stunden. In einer klinischen Studie mit 34 Glioblastompatienten hatten jene, die MRT-gesteuerten fokussierten Ultraschall zusammen mit Chemotherapie erhielten, ein medianes Gesamtüberleben von mehr als 30 Monaten, verglichen mit 19 Monaten in der Kontrollgruppe. Präklinische Modelle, auf die in einer im New England Journal of Medicine veröffentlichten Studie verwiesen wird, zeigten, dass fokussierter Ultraschall die Aducanumab-Zufuhr in die Zielregionen des Gehirns um das Fünf- bis Achtfache steigerte. Die Methode wurde sogar bei Kindern mit Hirntumoren erprobt, was ihre Praktikabilität bei pädiatrischen Patienten belegt.
Warum dieses Problem gravierender ist, als man denkt
Die globale Belastung durch neurologische Erkrankungen ist enorm und wächst weiter. Die durch neurologische Erkrankungen verursachten Behinderungen haben seit 1990 um 18 % zugenommen, angetrieben durch alternde Bevölkerungen und den Anstieg von Erkrankungen wie der diabetischen Neuropathie. Über 80 % der Todesfälle durch neurologische Erkrankungen ereignen sich in Ländern mit niedrigem und mittlerem Einkommen, wo selbst der Zugang zu Grundversorgung eingeschränkt ist.
Die Blut-Hirn-Schranke ist nicht nur ein Medikamentenzufuhrproblem. Sie ist der strukturelle Grund, warum die Neurologie der Kardiologie, der Onkologie und der Immunologie beim therapeutischen Fortschritt jahrzehntelang hinterherhinkt. Jedes andere Organ des Körpers ist modernen Pharmaka zugänglich auf eine Art, wie es das Gehirn schlicht nicht ist. Solange die Medikamentenzufuhr durch die Blut-Hirn-Schranke nicht im großen Maßstab gelöst ist, werden Milliarden von Menschen mit neurologischen Erkrankungen weiterhin mit einer Behandlungslücke konfrontiert sein, die kein noch so ausgefeiltes Wirkstoffdesign allein schließen kann.
Mehr als 3 Milliarden Menschen weltweit leben mit einer neurologischen Erkrankung, die nun die führende Ursache für behinderungsbereinigte Lebensjahre (DALYs) weltweit ist. Dennoch bleibt die Medikamentenzufuhr durch die Blut-Hirn-SchrankeEine selektive Membran, die kontrolliert, welche Stoffe aus dem Blutkreislauf ins Gehirn gelangen. Nanoplastik ist klein genug, um diese Barriere zu durchqueren und sich in Gehirngewebe anzusammeln. der limitierende Faktor der ZNS-Pharmakotherapie: Mehr als 98 % der niedermolekularen Wirkstoffe und praktisch 100 % der großmolekularen Therapeutika überwinden die Blut-Hirn-Schranke (BHS) nicht in therapeutischen Konzentrationen. Das ist keine weiche Statistik. Es ist die größte einzelne strukturelle Einschränkung in der Neuropharmakologie, und sie ergibt sich aus einer Schranke, deren molekulare Architektur gezielt dafür ausgelegt ist, genau jene Moleküle auszuschließen, auf die die moderne Medizin angewiesen ist.
Molekulare Architektur der Blut-Hirn-Schranke
Die BHS wird von spezialisierten Endothelzellen gebildet, die ZNS-Mikrogefäße auskleiden und durch Tight-Junction-Komplexe (TJ) verbunden sind, welche den parazellulären Spalt abdichten. Erstmals von Paul Ehrlich 1885 durch Farbstoffausschlussexperimente identifiziert, wurde die molekulare Grundlage der Schranke erst verstanden, als die Elektronenmikroskopie die kontinuierlichen TJ-Stränge zwischen Hirnendothelzellen sichtbar machte.
Der TJ-Komplex an der BHS wird von Claudin-5 dominiert, einem Tetraspan-Transmembranprotein, dessen extrazelluläre Schleifen homo- und heterotypische Wechselwirkungen mit Claudinen auf benachbarten Zellen eingehen. Der Claudin-5-Knockout in transgenen Mäusen erzeugt morphologisch normale Verbindungen, aber eine katastrophale Permeabilität für Moleküle unter 800 Da, was zu neonatalen Tod innerhalb von etwa 10 Stunden führt. Occludin und junktionale Adhäsionsmoleküle leisten zusätzliche strukturelle Verstärkung. Die funktionelle Konsequenz ist quantifizierbar: Der in-vivo-transendotheliale elektrische Widerstand (TEER) von Hirnmikrogefäßen beträgt 1.500 bis 2.000 Ohm pro Quadratzentimeter, gegenüber 3 bis 30 in peripheren Mikrogefäßen. Dieser 50-fache Unterschied in der parazellulären Dichtigkeit ist die physische Manifestation der Schranke.
Die Endothelzellen selbst unterscheiden sich von ihren peripheren Pendants in mehreren messbaren Eigenschaften. Sie sind 39 % dünner als muskuläre Endothelzellen, mit weniger als einem Viertel Mikrometer Abstand zwischen luminaler und abluminaler Oberfläche. Sie weisen drastisch reduzierte Transzytose-Raten auf, sind vollständig fenestrierungsfrei und exprimieren minimale Leukozyten-Adhäsionsmoleküle. Ihre Mitochondriendichte ist erhöht, was den Energiebedarf des aktiven Transports widerspiegelt.
Die neurovaskuläre EinheitMehrzelluläres System um Hirnkapillaren, bestehend aus Endothelzellen, Perizyten und Astrozyten, das die Blut-Hirn-Schranke bildet und aufrechterhält.
Die Barrierefunktion ist nicht den Endothelzellen allein eigen. Sie wird durch die neurovaskuläre Einheit (NVE) induziert und aufrechterhalten, eine multizellulare Anordnung aus Endothelzellen, Perizyten, Astrozyten, Basalmembran, Mikroglia und Neuronen.
Perizyten sind in der vaskulären Basalmembran mit einem Bedeckungsgrad von 1:1 bis 3:1 (Endothel:Perizyt) im ZNS eingebettet, verglichen mit 100:1 im Skelettmuskel. ZNS-Perizyten stammen einzigartig von der Neuralleiste und nicht vom Mesoderm ab; sie regulieren über PDGF-B/PDGFR-beta-Signalgebung mit Endothelzellen die TJ-Bildung, Transzytose-Raten und den Kapillardurchmesser. Perizytenverlust in Tiermodellen erhöht direkt die BHS-Permeabilität.
Astrozytäre perivaskuläre Endfüße bedecken über 99 % der Hirnmikrovaskulatur und bilden die Glia limitans perivascularis. Diese Endfüße exprimieren Aquaporin-4-Wasserkanäle und den Dystroglycandystrophin-Komplex, durch den sie an der Basalmembran verankert sind. Von Astrozyten stammende Signale, darunter Sonic hedgehog und Angiopoietin-1, erhalten die TJ-Proteinexpression und die Barrierepolarität aufrecht.
Warum die Medikamentenzufuhr durch die Blut-Hirn-Schranke scheitert
Die BHS schränkt die Medikamentenaufnahme durch drei überlappende Mechanismen ein: parazellulären Verschluss, transzelluläre Restriktion und aktiven Efflux.
Parazelluläre Okklusion
TJ-Komplexe blockieren den Durchtritt hydrophiler Moleküle durch den interendothelialen Spalt. Nur die passive Diffusion fettlöslicher Moleküle unter etwa 400 bis 600 Da ist erlaubt. Diese Molekulargewichtsgrenze schließt praktisch alle Biologika aus (Antikörper bei ~150 kDa, Antisense-Oligonukleotide bei ~7 kDa, virale Vektoren bei Millionen Da) und die meisten synthetischen Kleinmoleküle.
Efflux-Transport
Selbst lipophile Wirkstoffe, die die Endothelzellmembran überwinden, sind aktivem Ausstrom ausgesetzt. P-GlykoproteinEine Proteinpumpe in den Wänden von Hirnkapillaren, die Wirkstoffe aktiv ins Blut zurückbefördert und so ihre Anreicherung im Hirngewebe verhindert. (P-gp/MDR1), das Brustkrebsresistenzprotein (BCRP) und multidrug-resistenzassoziierte Proteine (MRPs) sind ABC-Kassetten-Efflux-Transporter, die zur luminalen Oberfläche polarisiert sind. P-gp allein hat eine außerordentlich breite Substratspezifität, und neue Erkenntnisse zeigen, dass es die Hirnkonzentrationen mehrerer Antidepressivaklassen begrenzt und zum Therapieversagen beiträgt.
Im Krankheitszustand kann der Efflux zunehmen. Etwa ein Drittel der Epilepsiepatienten ist pharmakoresistent, und P-gp-Überexpression in epileptogenem Gewebe ist ein dokumentierter Faktor. Die Schranke verhindert nicht nur den Eintritt von Wirkstoffen; sie entfernt sie aktiv aus dem ZNS-Kompartiment nach dem Eintritt.
Die klinischen Konsequenzen
Diese Mechanismen kumulieren zu ernüchternden klinischen Ergebnissen. Die Phase-2/3-Misserfolgsrate für ZNS-Wirkstoffe liegt bei etwa 85 %, nur von der Onkologie übertroffen. Die klinische Zulassungsrate beträgt 6,2 %, die Hälfte der 13,3 % für Nicht-ZNS-Therapeutika. Entwicklungszeiträume sind 12,8 Monate länger. Das wirtschaftliche Signal ist eindeutig: Mehrere große Pharmaunternehmen haben die ZNS-Wirkstoffentwicklung vollständig aufgegeben.
Das Antikörper-Pharmakokinetik-Problem
Monoklonale Antikörper sind die weltweit am schnellsten wachsende Wirkstoffklasse, aber ihr Molekulargewicht (~150 kDa) liegt etwa 375-mal über der Grenze für passive Diffusion durch die BHS. Die Hirnaufnahme peripher verabreichter Antikörper liegt typischerweise bei weniger als 0,1 % der injizierten Dosis.
Diese pharmakokinetische Realität prägt die gesamte Alzheimer-Antikörperstrategie. Lecanemab und Aducanumab erfordern hochdosierte intravenöse Infusionen, um überhaupt marginale Hirnkonzentrationen zu erreichen. Die dosislimitierende Toxizität, ARIA (amyloidbedingte Bildgebungsanomalien einschließlich Ödeme und Mikroblutungen), ist zum Teil ein Artefakt der durch die schlechte BHS-Penetration erzwungenen systemischen Überdosierung. Das therapeutische Fenster ist eng, nicht weil die Zielbiologie falsch ist, sondern weil der gelieferte Anteil verschwindend gering ist.
Aufkommende Strategien: Die Biologie der Schranke nutzen
Rezeptorvermittelte TranszytoseProzess, bei dem Moleküle an Zelloberflächenrezeptoren binden und in Vesikeln durch die Zelle transportiert werden, um Wirkstoffe ins Gehirn zu schleusen. (RMT)
Die BHS exprimiert eine Reihe von Rezeptoren, die physiologisch essentielle Makromoleküle vom Blut ins Gehirn transportieren. Die rezeptorvermittelte Transzytose nutzt diese Wege, indem therapeutische Fracht so entwickelt wird, dass sie RMT-Rezeptoren bindet, Internalisierung, endosomale Sortierung und abluminale Freisetzung auslöst.
Der Transferrinrezeptor (TfR) ist das klinisch am weitesten fortgeschrittene Ziel. Die Transport-Vehicle-Plattform von Denali Therapeutics modifiziert Fc-Domänen zur TfR-Bindung, was die Transzytose angehängter therapeutischer Proteine ermöglicht. Dieser Ansatz hat Phase-1-Studien für die Iduronat-2-Sulfatase-Zufuhr beim Hunter-Syndrom und den Progranulin-Ersatz bei frontotemporaler Demenz erreicht. Roches Brain-Shuttle-Programm konjugiert Anti-TfR-Antikörper mit Anti-Amyloid-beta-Antikörpern oder Neprilysin und demonstriert ZNS-Zufuhr sowie Amyloidreduktion in präklinischen Modellen.
Weitere untersuchte RMT-Ziele umfassen CD98hc (SLC3A2), den Insulinrezeptor, IGF1R/IGF2R und TMEM30A. Jedes weist unterschiedliche Kompromisse hinsichtlich BHS-Spezifität, luminaler Zugänglichkeit und Ladekapazität auf. Das Fachgebiet konvergiert auf das Prinzip, dass Affinitätsabstimmung entscheidend ist: hochaffine TfR-Binder werden in Endosomen gefangen und abgebaut, während moderat-affine Binder effizienter ins Hirnparenchym freigesetzt werden.
Fokussierter Ultraschall (FU)
MRT-gesteuerter fokussierter Ultraschall in Kombination mit systemisch verabreichten Mikrobläschen erzeugt eine vorübergehende, lokalisierte BHS-Öffnung durch mechanische Oszillation der Mikrobläschen gegen die Endothelwand. Dabei werden TJ-Proteine verdrängt, ohne dauerhafte strukturelle Schäden zu verursachen, und es entsteht ein mehrstündiges Fenster für die Medikamentenaufnahme.
Die klinischen Ergebnisse sind überzeugend. Beim Glioblastom zeigten 34 Patienten unter FU-verstärkter Chemotherapiezufuhr ein medianes progressionsfreies Überleben von fast 14 Monaten gegenüber 8 Monaten in der Kontrollgruppe, mit einem Gesamtüberleben von über 30 Monaten gegenüber 19. Die im NEJM veröffentlichte Aducanumab-Studie zitiert präklinische Belege für eine 5- bis 8-fach erhöhte Antikörperzufuhr in beschallte Hirnregionen und zeigte eine signifikant stärkere Amyloidreduktion in behandelten gegenüber unbehandelten Regionen über 26 Wochen. Die Machbarkeit wurde bei pädiatrischen Patienten mit diffusen Mittelliniengliomen demonstriert.
Die Überwachung akustischer Emissionen liefert nun einen Echtzeit-Biomarker für das Ausmaß der BHS-Öffnung und ermöglicht die Dosistitrierung der Ultraschallexposition.
Das Ausmaß des Problems
Die WHO-Analyse von 2024 der Global-Burden-of-Disease-Daten ergab, dass neurologische DALYs seit 1990 um 18 % gestiegen sind, wobei über 80 % der neurologischen Todesfälle in Ländern mit niedrigem und mittlerem Einkommen konzentriert sind. Die Zahl der diabetischen Neuropathiefälle hat sich mehr als verdreifacht. Die zehn führenden neurologischen Erkrankungen nach Krankheitslast umfassen Schlaganfall, Demenz, Epilepsie und Nervensystemkarzinome, die alle ZNS-gängige Therapeutika erfordern, welche die BHS systematisch ausschließt.
Die Blut-Hirn-Schranke ist nicht nur eine Herausforderung für die Medikamentenzufuhr. Sie ist die strukturelle Erklärung dafür, warum die Neurologie langsamer vorangeschritten ist als jede vergleichbare medizinische Disziplin. Die Kardiologie hat Stents und Statine. Die Onkologie hat Checkpointinhibitoren und CAR-T-Zellen. Die Immunologie hat Biologika, die Autoimmunerkrankungen transformiert haben. Jede dieser Revolutionen hing davon ab, dass Wirkstoffe ihr Zielgewebe erreichen. Das Gehirn bleibt, durch biologisches Design, das am schwersten erreichbare Organ des Körpers. Solange die Medikamentenzufuhr durch die Blut-Hirn-Schranke nicht im großen Maßstab gelöst ist, wird die Behandlungslücke zwischen neurologischen Erkrankungen und dem Rest der Medizin fortbestehen.